|
近日,我校科研技术中心(新安医学教育部重点实验室)徐奎研究员团队在国际生物材料顶级期刊《Biomaterials》(IF=14.0,中科院TOP一区)上发表了骨缺损修复相关学术论文。论文第一作者及第一通讯作者为徐奎研究员,浙江大学医学院附属第一医院陈威震助理研究员和深圳市人民医院生物医学工程研究院院长张其清教授为该论文共同通讯作者。我校为第一完成单位和第一通讯单位。

影响新植入材料与周围天然骨组织完美融合的因素有很多。外部因素通常由手术引起,如微生物感染和氧化应激。一旦致病生物膜形成,一个直接的结果是将植入物与骨组织的相互作用隔离开来。更重要的是,来自细菌的大量酸性代谢物积聚在骨与植入物的界面,形成了一个有利于破骨细胞而不是成骨细胞的微环境。过多的活性氧产生是植入手术中另一个几乎不可避免的外部因素。积累的活性氧引起的氧化应激会严重破坏参与成骨的细胞的功能,阻止新骨组织的形成。导致植入物不能与周围骨组织整合的直接内在因素是骨稳态紊乱。骨重塑是一个密切协调的过程。在该过程中,旧的或受损的骨组织被破骨细胞移除,同时被新形成的骨组织所取代。但这种平衡很容易被打破。细胞衰老、细胞凋亡和氧化应激诱导的DNA损伤都是导致骨稳态失衡的原因。事实上,几乎不可能找到一种具有生物多用途表面的植入物。例如骨科临床常用的钛基植入物和聚醚醚酮材料,其抗菌、抗氧化性能以及促进成骨、抑制破骨细胞生成的能力都非常薄弱。尽管生物活性涂层的开发一直被认为是弥补这些植入物缺陷的有效方法,但无论是涂层沉积技术还是涂层的生物功能都未能达到人们的期望。
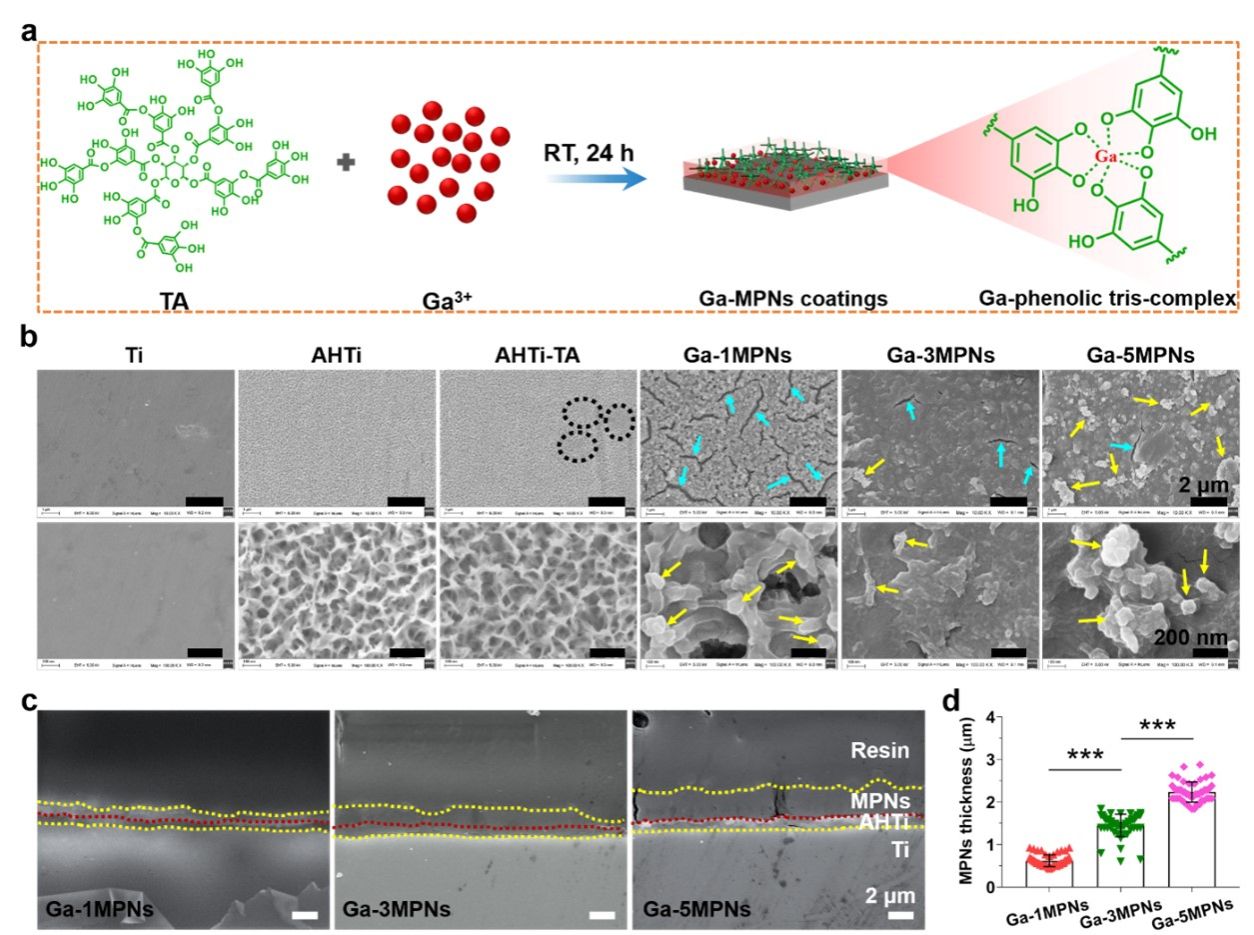
综上,考虑种植体在体内所面临的多重挑战,设计新的种植体涂层具有重要意义。在本研究中,作者通过将植入物浸入单宁酸和镓离子的混合溶液中制备了一种基于镓(III)-酚醛网络的多功能涂层。该涂层具有优异的近红外光热性能。涂层降解可释放低浓度的单宁酸和镓离子进入周围微环境中,而且在酸性和氧化应激微环境中释放速度更快。光热性能以及释放的单宁酸和镓离子使涂层具有出色的广谱抗菌能力。此外,涂层有效地降低了成骨细胞内的活性氧。体外和体内实验表明,该涂层通过促进骨生成和抑制破骨细胞生成增强了钛种植体的骨整合能力。本研究为骨植入体多功能生物活性涂层的开发提供了一种切实可行的方法。
|